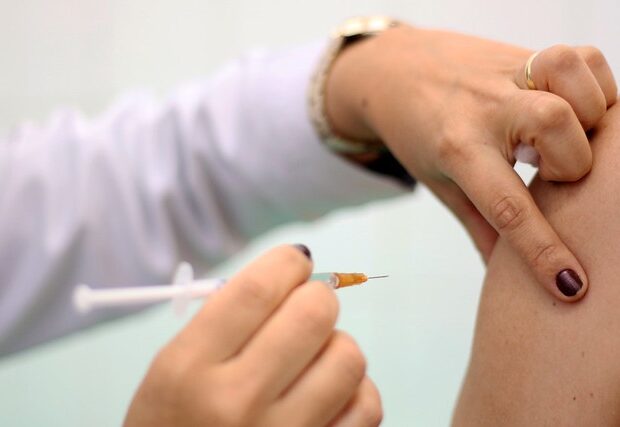
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta quarta-feira (6/5) a nova composição das vacinas da gripe que serão usadas no Brasil em 2026. Essa decisão aconteceu durante a 7ª Reunião Pública da Diretoria da Anvisa e segue as orientações da Organização Mundial da Saúde (OMS) para o Hemisfério Sul.
A gripe é uma doença que afeta o sistema respiratório, causada por vírus que se espalham facilmente, especialmente em épocas do ano específicas. A cada ano, a fórmula da vacina é atualizada para proteger melhor contra os vírus que estão circulando. A diretora Daniela Marreco, que apresentou a proposta, ressaltou dados importantes: até 18 de abril de 2026, as internações por gripe subiram quase 93%, e as mortes aumentaram 10% em comparação ao ano anterior.
Além disso, a diretoria da Anvisa aprovou melhorias no processo de análise de medicamentos e produtos biológicos para acelerar a aprovação de pesquisas clínicas e registros. Daniela Marreco destacou que o prazo para o atendimento das exigências agora é de 60 dias, ajudando a tornar o processo mais rápido.
Outra mudança aprovada foi a atualização de regras para análises regulatórias, tornadas mais eficientes e com menos burocracia, trazendo maior segurança e previsibilidade para o mercado.
A Anvisa também iniciou um projeto-piloto de avaliação técnica online para facilitar a análise de documentos relacionados a insumos farmacêuticos.
Além disso, foram atualizadas as listas de substâncias controladas e revisadas regras para ingredientes de agrotóxicos e produtos de limpeza, visando maior segurança e controle.
Por fim, discutiu-se uma proposta para novas regras de importação e controle de qualidade de insumos para farmácias de manipulação, com mais análises a serem feitas nos próximos passos.